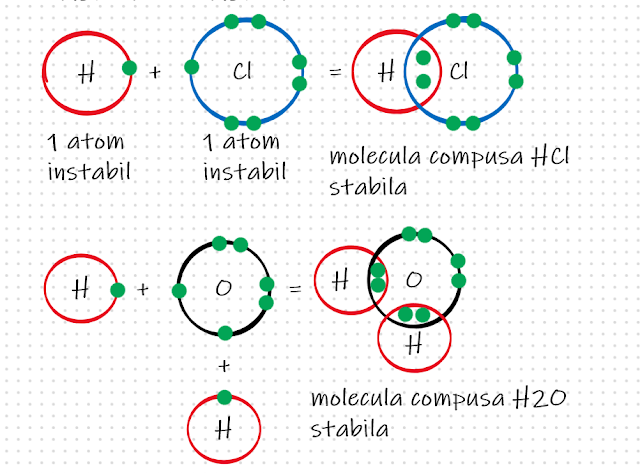
Uneori aceste reacții redox sunt nedorite, de exemplu coroziunea metalelor.
Ramura chimiei care studiază procesele redox se numește electrochimie.
Reacțiile redox sunt reacții chimice care au loc cu modificarea numărului de oxidare al unuia sau a mai multor elemente din componența reactanților.
Un proces redox poate fi recunoscut prin variaţia numerelor de oxidare ale unor elemente sau grupe de elemente.
Numărul de oxidare reprezintă numărul de electroni proprii implicaţi în formarea legături chimice.
N.O. = sarcini reale (la ioni) sau formale (la atomi/molecule).
Reguli de stabilire a N.O.:
1. Substanțele în stare liberă au NO=0
ex: H20, Cl20, O20, Cu0, Fe0, etc.
2. Numărul de oxidare al hidrogenului este:
☆+1 în
majoritatea compuşilor.
Exemplu:
H+1Cl, H2+1O , H+1NO3
☆ excepție: într-o hidrură metalică (compus al hidrogenului cu un metal),
numărul lui de oxidare fiind atunci -1.
Exemplu:
NaH-1, CaH2-1
3.
Numărul de oxidare al oxigenului
este :
☆ -2 în majoritatea compuşilor.
Exemplu: H2O-2, NaO-2H, HNO-23
☆ -2 în majoritatea compuşilor.
Exemplu: H2O-2, NaO-2H, HNO-23
☆ excepție: în cazul peroxizilor (atunci este -1)
Exemplu:
H2O-12, Na2O-12
4. Numărul de oxidare al fluorului într-o moleculă (cu excepția moleculei de F2) este întotdeauna -1.
4. Numărul de oxidare al fluorului într-o moleculă (cu excepția moleculei de F2) este întotdeauna -1.
Exemplu:
HF-1, NaF-1 .
5. În compuşi, numărul de oxidare al elementelor din grupa IA este +1.
Exemplu: Na+1Cl, Na+1OH, K+12O.
6. În compuşi, numărul de oxidare al elementelor din grupa IIA este +2.
Exemplu: Mg+2Cl2, Ca+2O.
7. Numărul de oxidare al unui ion este egal cu sarcina sa.
Exemplu: (HO)-1, (SO4)-2, (NO3)-1, (PO4)-3 .
8. Suma algebrică a numerelor de oxidare a elementelor ce formează un compus neutru este egală cu zero.
Exemplu: Într-o moleculă de H2SO4 (acid sulfuric), suma numerelor de oxidare ale hidrogenului, sulfului si oxigenului este zero.
H+12SXO-24 ⇒2∙(+1) +1∙x + 4∙(-2) = 0 ⇒ x = +6
H+12S+6O-24 .
5. În compuşi, numărul de oxidare al elementelor din grupa IA este +1.
Exemplu: Na+1Cl, Na+1OH, K+12O.
6. În compuşi, numărul de oxidare al elementelor din grupa IIA este +2.
Exemplu: Mg+2Cl2, Ca+2O.
7. Numărul de oxidare al unui ion este egal cu sarcina sa.
Exemplu: (HO)-1, (SO4)-2, (NO3)-1, (PO4)-3 .
8. Suma algebrică a numerelor de oxidare a elementelor ce formează un compus neutru este egală cu zero.
Exemplu: Într-o moleculă de H2SO4 (acid sulfuric), suma numerelor de oxidare ale hidrogenului, sulfului si oxigenului este zero.
H+12SXO-24 ⇒2∙(+1) +1∙x + 4∙(-2) = 0 ⇒ x = +6
H+12S+6O-24 .
Exemple:
》 H2CO3.
H+12CXO-23 ⇒2∙(+1) +1∙x + 3∙(-2) = 0 ⇒ x
= +4
H+12C+4O-23 .
》 HNO3
H+1NXO-23 ⇒1∙(+1) +1∙x + 3∙(-2) = 0 ⇒ x
= +5
H+1N+5O-23 .
》 NO2
NXO-22⇒1∙x + 2∙(-2) = 0 ⇒ x
= +3
N+3O-22
.
》 KMnO4
K+1MnXO-24 ⇒1∙(+1) +1∙x + 4∙(-2) = 0 ⇒ x
= +7
K+1Mn+7O-24 .
》 K2Cr2O7
K+12CrX2O7 ⇒ 2∙(+1) +2∙x + 7∙(-2) = 0 ⇒ x
= +6
K+12Cr+62O7